医疗器械唯一标识(UDI)的起源可以追溯到2013年。那一年,国际医疗器械监管机构论坛(IMDRF)发布了一份指南,名为《医疗器械唯一标识系统指南》,这标志着UDI系统的诞生。同年,美国也开始实施医疗器械唯一标识系统,并要求企业在7年内全面实施。

UDI系统的重要性
UDI系统的重要性在于它为医疗器械产品提供了全球唯一的识别码,类似于人的身份证,可以实现全链条医疗器械的通查通识。这有助于加强全生命周期的管理,提升监管效能。UDI系统还可以提高医疗器械不良事件报告的质量,更有效地识别产品问题,更迅速地召回问题器械,以确保患者的安全。
UDI系统的组成
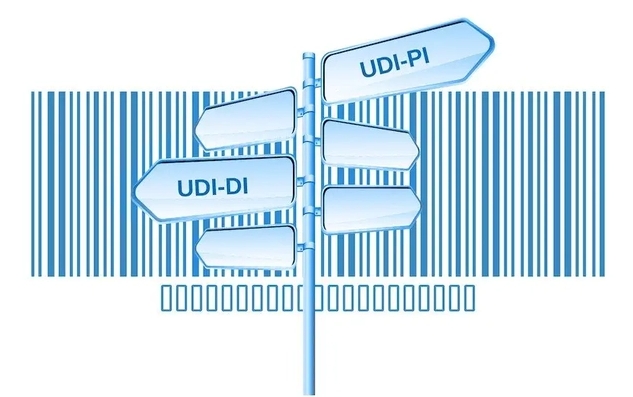
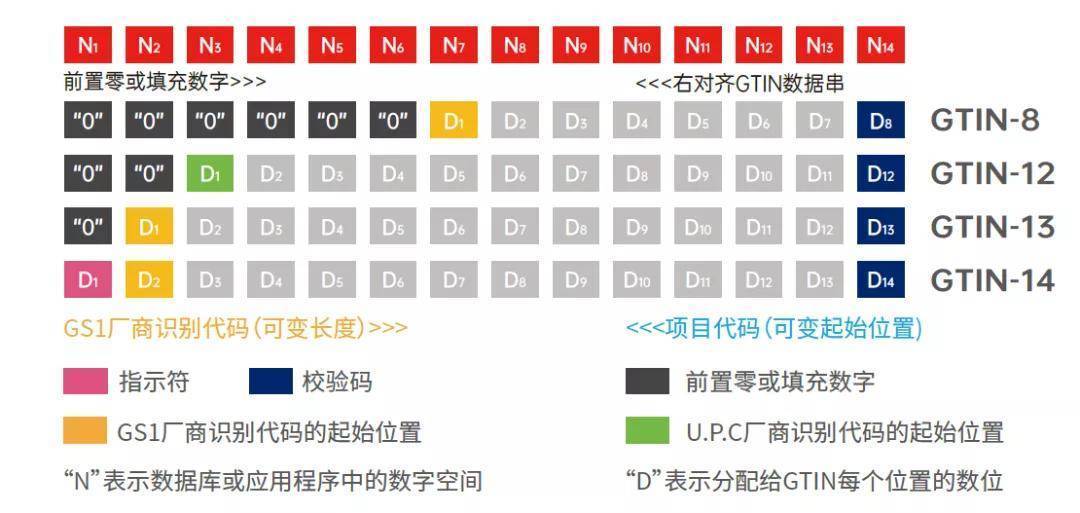
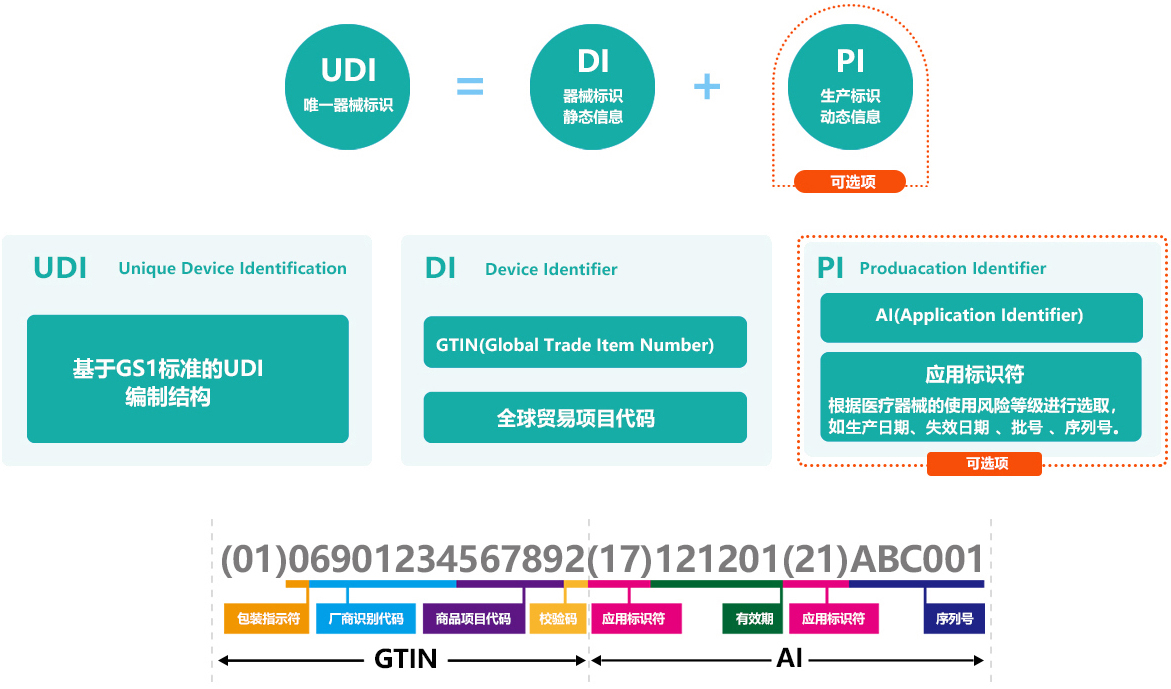
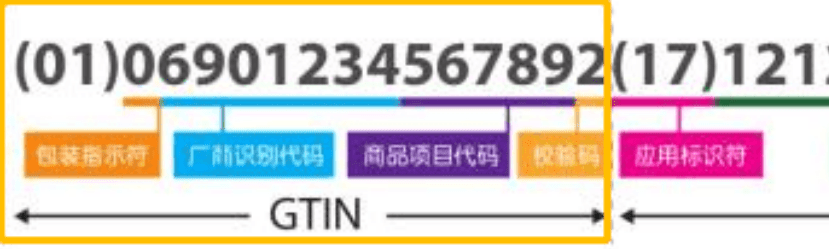
UDI系统由医疗器械唯一标识、数据载体和数据库组成。医疗器械唯一标识是由产品标识(DI)和生产标识(PI)两部分组成的。产品标识为识别注册人/备案人、医疗器械型号规格和包装的唯一代码;生产标识则包含了医疗器械生产过程相关信息的代码,如医疗器械序列号、生产批号、生产日期、失效日期等。
UDI系统在中国的发展
中国在2019年8月发布了《医疗器械唯一标识系统规则》,并于2019年10月1日起开始施行。中国的UDI系统建设借鉴了国际标准,遵循政府引导、企业落实、统筹推进、分步实施的原则。最初,第一批实施医疗器械唯一标识的工作被推迟到2021年1月1日。此后,UDI系统的实施范围逐渐扩大,到2024年6月1日起,所有的医疗器械都需要具有医疗器械唯一标识。
UDI系统的国际影响
UDI系统不仅是美国和中国的监管要求,也在全球范围内得到推广和应用。例如,在欧洲,医疗器械唯一标识是欧洲医疗器械可追溯性的关键组成部分, UD I的概念在2013年的IMDRF指南中就已经提出。这表明,UDI系统已经成为全球医疗器械监管的一个重要工具。
总的来说,医疗器械唯一标识(UDI)的起源可以追溯到2013年,随着全球范围内对医疗器械安全和有效性的关注度不断提高,UDI系统的重要性也在逐渐增加。
 UDI网-UDI申请编码赋码软件专业知识网
UDI网-UDI申请编码赋码软件专业知识网